大家好,欢迎来看今天的文献解读!你是否对特发性肺纤维化(IPF)的病理机制充满好奇?在这篇研究中,作者们通过单细胞转录组测序和机器学习的结合,深入探索了IPF肺组织中的巨噬细胞亚群,揭示了它们的分子特征及其潜在的诊断标志物。这不仅让我们对IPF的免疫调节机制有了新的认识,还为未来的治疗策略提供了新的思路。想知道这些新发现会如何影响IPF的诊断和预后吗?让我们一起深入探讨吧!
这篇文章的研究亮点在于,作者通过高维加权基因共表达网络分析(hdWGCNA)识别出了与IPF相关的巨噬细胞亚群,特别是一个名为ATP5-MΦ的亚群,这种亚群在IPF肺组织中特有,且与能量代谢相关。此外,作者还采用机器学习方法构建了预测模型,以评估这些巨噬细胞特征基因对IPF患者预后的影响。这项研究不仅是对IPF病理机制的深入剖析,也是首次结合单细胞分析和机器学习来识别巨噬细胞亚群和相关生物标志物的尝试,具有很大的创新性和前瞻性。
数据来源
本研究的数据主要来自**Gene Expression Omnibus (GEO)**数据库,具体使用了以下数据集:
GSE128033:包括10个正常样本和8个IPF样本(总计66,500个细胞)。
GSE32537:39个正常样本与131个IPF样本用于构建模型。
GSE110147:11个正常样本与22个IPF样本用于模型的验证。
题目:IPF-related new macrophage subpopulations and diagnostic biomarker identification - combine machine learning with single-cell analysis
杂志:Respiratory Research
拆解部分
巨噬细胞在特发性肺纤维化中的角色
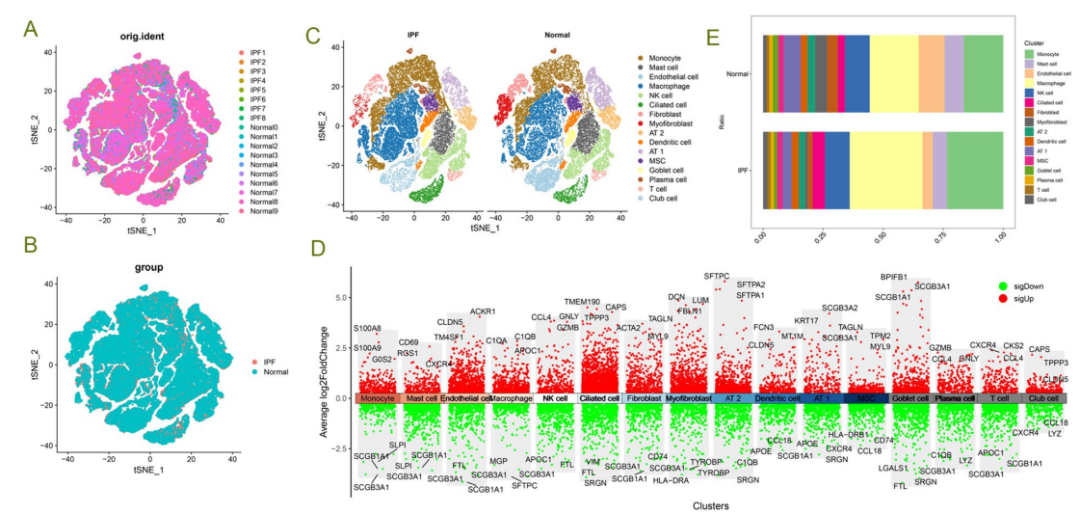
图1展示了正常与特发性肺纤维化(IPF)患者肺组织中巨噬细胞亚群的比例变化。通过t-SNE图像,可以清晰地观察到细胞在正常与纤维化肺组织中的分布差异。研究显示,IPF患者的巨噬细胞显著增加,伴随纤维母细胞和AT1细胞的减少。这一发现提示巨噬细胞在IPF的病理过程中可能发挥了重要作用,特别是C1QA和C1QB的上调与免疫调节及炎症反应密切相关。

在图2中,进一步分析了IPF肺组织中巨噬细胞的异质性,该图揭示了巨噬细胞被分为13个亚簇,其中Cluster 0被识别为与IPF相关的巨噬细胞(IPF-MΦ),而Cluster 11则仅在IPF组织中存在。这表明IPF-MΦ在炎症及纤维化过程中可能扮演独特角色,尤其是与氧化磷酸化相关的ATP5基因的高表达,可能与其代谢重编程密切相关。
IPF-MΦ的细胞间通信与基因模块分析
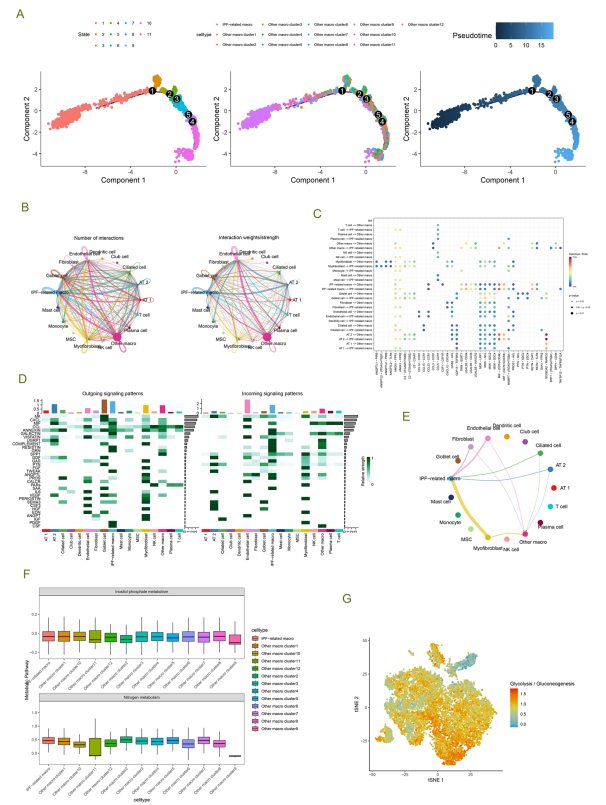
图3通过伪时间轨迹分析展示了IPF-MΦ在巨噬细胞分化中的关键角色。CellChat分析显示,IPF-MΦ与其他细胞类型之间的紧密通信,尤其与巨噬细胞之间的强相互作用,可能对病理发展起到重要作用。这种增强的细胞间通信可能加剧了IPF的炎症及纤维化过程,强调了IPF-MΦ在调控细胞微环境中的中心角色。
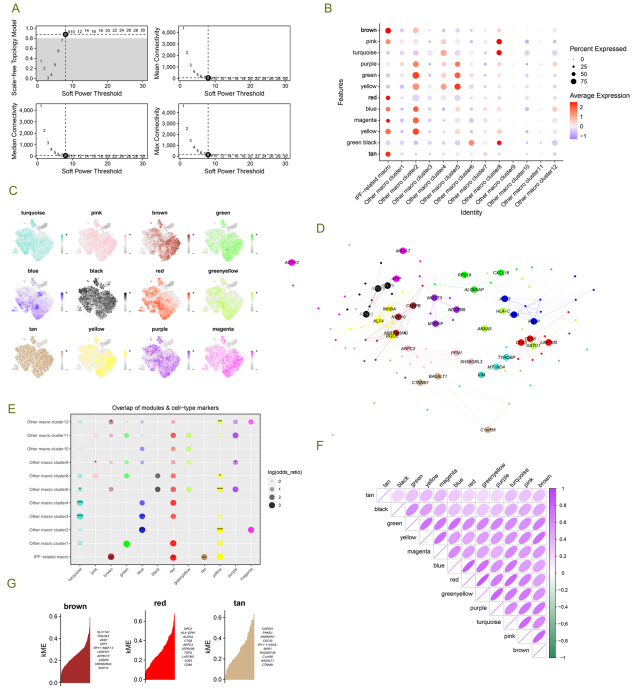
在图4中,采用高维加权基因共表达网络分析(hdWGCNA)识别了模块核心基因。识别出的红色、棕色和黄色模块核心基因在IPF-MΦ中的显著表达,提示其在IPF进展中可能扮演关键角色。通过构建蛋白质-蛋白质相互作用(PPI)网络,进一步揭示这些基因在巨噬细胞功能中的潜在作用,为理解IPF相关巨噬细胞的分子机制提供了重要信息。
关键基因的识别与预后分析
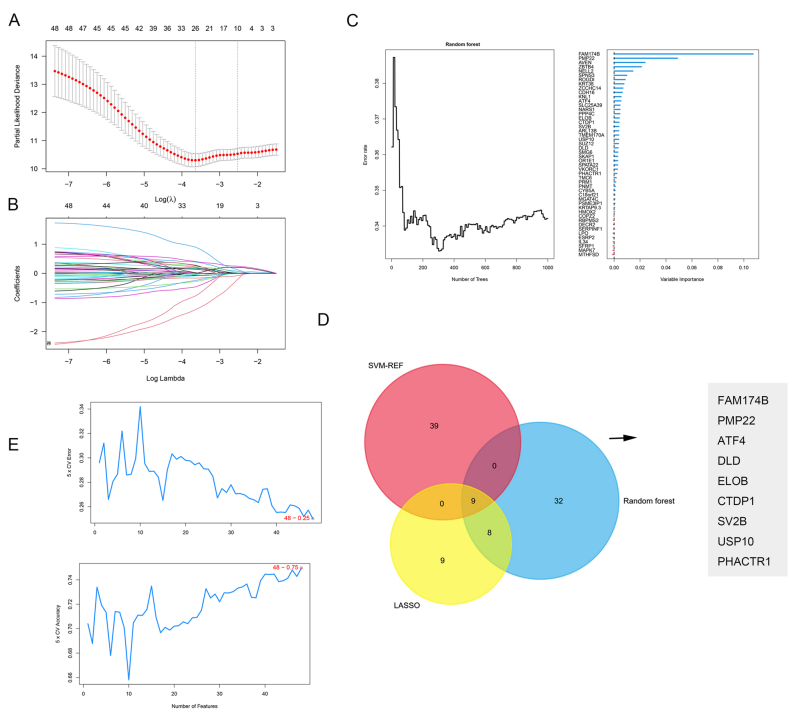
图5展示了通过多种机器学习方法识别出的与IPF相关的关键基因。这些基因的功能可能与炎症反应、细胞代谢等密切相关,结合不同算法的结果,为IPF患者的预后提供了有效的生物标志物。
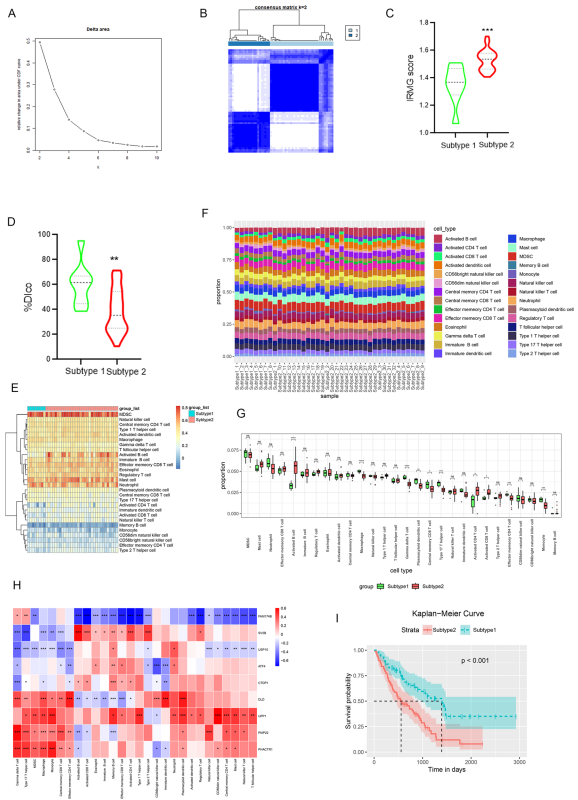
图6则通过CDF曲线分析评估了不同亚型IPF患者的生物特征,显示出IRMG评分与肺功能的显著差异,提示高IRMG评分组可能伴随更严重的疾病进程。这种免疫状态的变化可能影响疾病的发展及患者对治疗的反应,强调了个体化治疗的重要性。
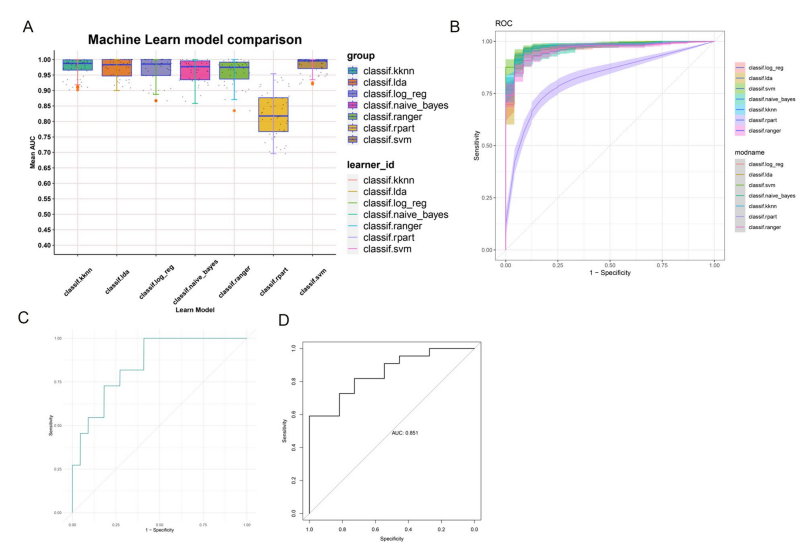
在图7中,基于机器学习算法构建的IPF预测模型,表明支持向量机(SVM)算法在准确性、灵敏度和特异性上表现最佳,为IPF患者的早期识别和干预提供了科学依据。
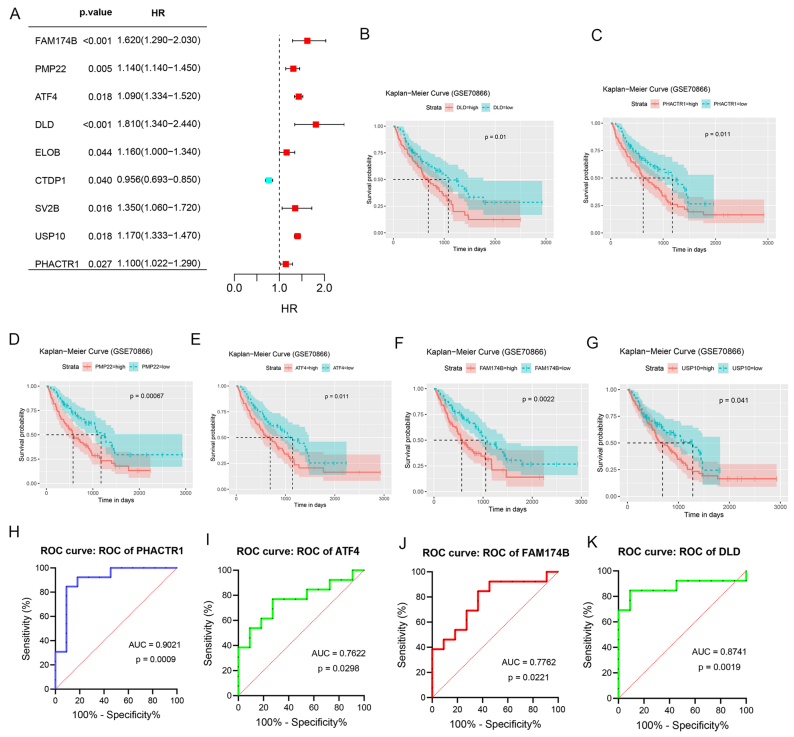
最后,图8通过单变量Cox回归分析确定了与IPF患者预后相关的基因,这些基因的功能研究将进一步阐明其在IPF病理中的具体作用,推动个性化医疗的发展。
总结
这项研究聚焦于特发性肺纤维化(IPF)中的巨噬细胞亚群,通过结合单细胞转录组测序和机器学习,揭示了巨噬细胞在IPF的病理机制中的重要性。研究中,作者识别出一个特有的巨噬细胞亚群ATP5-MΦ,并通过高维加权基因共表达网络分析(hdWGCNA)确定其在能量代谢中的作用。此外,利用机器学习方法,研究构建了预测模型,评估这些巨噬细胞特征基因对IPF患者预后的影响。研究结果不仅提供了新的诊断标志物,也为个体化治疗策略的制定奠定了基础,展示了巨噬细胞在IPF发展过程中的潜在关键角色。