【摘要】目的 基于深度学习方法训练模型,研究其用于腹部CT图像上分割胆囊并自动测量的可行性。方法 从本院 PACS 系统搜集2016年1月12日至2021年5月28日行腹部CT检查的患者,从中选取1154位患者的1181次CT检查图像,共得到2559个图像序列用于训练模型。由2位影像科医师标注胆囊,将全部数据按8:1:1的比例随机分为训练集(training set,n=2042)、调优集(validate set,n=245)和测试集(test set,n=271),训练3D U-net模型分割胆囊并自动测量。另搜集2022年9月10-19日的腹部CT扫描图像,随机选取共141位患者的141次检查的2
70个图像序列作为外部验证数据集。以外部验证集的预测结果评价模型的效能。使用Dice 相似系数(dice similarity coefficient, DSC)、体积相似度(volume similarity,VS)和Hausdorff距离(hausdorff distance,HD)定量评价模型分割胆囊区域的效能。使用Bland-Altman分析评价模型自动测量的胆囊体积、径线、平均CT值与医师标注测量值的一致性。结果 外部验证集的DSC中位数为0.980(0.970,0.980),VS为0.990(0.990,1.000),HD为1.69 (1.27,2.45)mm,各数据集之间DSC
、VS和HD的差异均有统计学意义(全部P<0.001)。外部验证集中对模型预测和医师标注测量结果进行了Bland-Altman分析,在考虑抽样误差的情况下体积、CT值、三维径线的95%一致性界限(limits of agreement, LoA)的可信区间分别为(-2.07,3.36)、(-1.55,1.15)、(-1.28,1.47)、(-3.34,4.07)和(-1.11,2.15),分别有2.6%、3.7%、3.7
%、1.1%和3.7%的点落在95%LoA以外。结论 基于深度学习模型可在腹部CT图像上自动分割胆囊区域,是将来进一步胆囊病变智能诊断的基础。
【关键词】 深度学习;胆囊;CT;人工智能;图像分割
胆囊是人体消化系统中的一个重要器官,它的主要功能是储存和释放胆汁,以帮助消化和吸收脂肪。但是,胆囊也是一个容易发生疾病的器官,常见的疾病包括胆囊结石、胆囊炎、胆囊癌等。有些胆囊疾病是因上腹部疼痛等症状而就诊,影像检查容易发现。有些胆囊疾病则是在上腹部CT检查中偶然发现的。由于腹部CT检查量日益增加,腹部脏器疾病多样、复杂,影像科医生浏览CT图像时要关注很多种疾病,可能会漏诊胆囊疾病。
近年来,随着人工智能(artificial intelligence,AI)技术的不断发展,AI辅助诊断已经成为了医疗领域的一个热点研究方向。既往研究显示在腹部CT的诊断中AI方法可以通过自动化图像分析和识别减少医生的工作量,并提高诊断准确性如在脏、肾上腺、胰腺、肝脏等脏器,但在胆囊的应用较少见到报道。
要实现胆囊的AI辅助诊断,首先需要进行胆囊图像分割,即将胆囊区域从CT图像中分离出来。由于胆囊的位置和形态不稳定,加之图像噪声的存在,胆囊图像分割存在一定的挑战。本研究的目的是测试使用深度学习方法进行胆囊分割的可行性,为进一步使用AI诊断胆囊疾病提供技术基础。
材料与方法
本研究为回顾性研究,获得了医院伦理委员会的批准[批件号:2019(168)],按照本单位人工智能AI模型训练规范执行研究方案。
1、用例定义
根据本单位人工智能AI项目管理方法,首先定义研发腹部CT图像胆囊分割模型的用例,包括AI模型的名称、临床问题、场景描述、模型在实际工作中的调用流程、模型输入输出数据规范等。
2、回顾队列建立
分两批从本院 PACS 系统搜集影像资料。第一批为2016年1月12日至2021年5月28日的腹部CT检查图像,用于训练模型;第二批为2022年9月10日至19日的腹部CT检查图像,用于外部验证。入组标准:检查项目为“腹部CT平扫”。排除标准:①图像中未包括完整胆囊;②
因患者配合欠佳、或者体位因素造成图像质量过差。共得到1154位患者1181次CT检查的2559个图像序列用于模型训练,141位患者的141次CT检查的270个图像序列用于外部验证(图 1)。
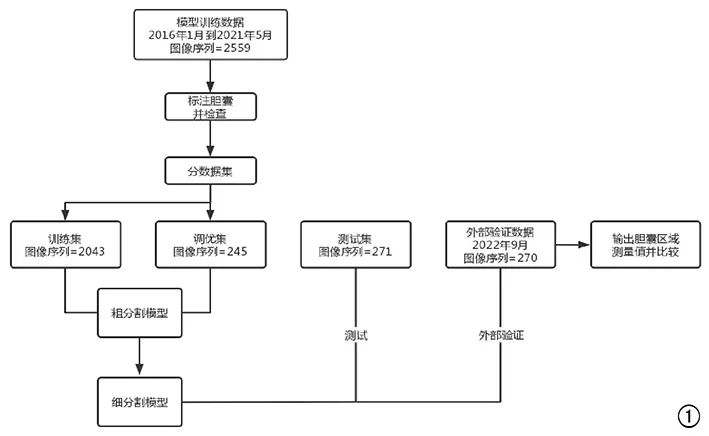
图 1 研究流程图
3、图像标注
将 DICOM 格式的图像转换为 NIFTI 格式。标注者使用ITK-SNAP(version3,Philadelphia,PA)软件标注胆囊区域(label)。由两位影像科医师标注,并由1位高年资腹部影像专业医师检查。标注范围包括完整的胆囊区域如胆囊内有可见病变,也应标注在胆囊范围内。对胆囊切除术后的情况,如果无可见胆囊则不标注,如有胆囊区域有明确的胆囊管代偿性扩张,则标注在胆囊范围内(图2)。
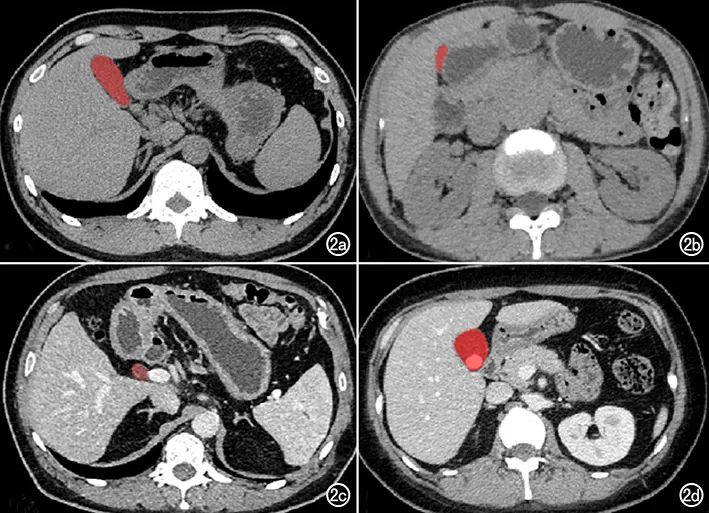
图
2 胆囊标注示意图,红色为标注区域。a)正常胆囊; b)餐后胆囊;c)胆囊切除术后扩张的胆管;d)胆囊及结石。
4、模型训练
将1154位患者的2559个图像序列按8:1:1的比例随机分为训练集 (n=2043)、调优集(n=245)和测试集(n=271)。深度学习的模型为3D U-Net,分为两步训练分割模型(图 1)。首先,在腹部范围内分割出胆囊大致范围(粗分割),再进一步在这个范围内精细分割出胆囊(细分割)。图像预处理时将图像分辨率设置为128×160×64(x,y,z),图像扩增采用随机噪声、平移、左右翻转、透视变换等方法。梯度下降使用ADAM优化算法,初始学习率(learning rate)设为1×10-3,每次读取的图像数量(batch size)为 4。训练次数(epoch)为400。模型训练的硬件为GPU NVIDIA Tesla P100 16G,程序语言为Python,软件环境包括Python3.6、Pytorch 0.4.1、Opencv、Numpy、SimpleITK等。
5、模型评价
模型输出结果为胆囊区域的预测范围(plabel)。计算plabel
全部体素的体积、平均CT值为胆囊的体积和平均CT值。以最小包围盒(minimum bounding box)法计算plabel的三维径线为胆囊的径线。使用Dice 相似系数(dice similarity coefficient, DSC)、体积相似度(volume similarity,VS)和Hausdorff距离(hausdorff distance,HD)定量评价模型分割胆囊区域的效能。
6、统计方法
使用R4.1.0软件进行统计分析。符合正态分布的计量资料以均值±标准差表示,不符合正态分布的连续变量表示为中位数(四分位间距),计数资料和等级资料以“数值(频率)”描述。使用方差分析比较各数据集间DSC、VS和HD的差异。使用Bland-Altman检验评价模型与专家测量值的一致性。P<0.05认为差异有统计学意义。
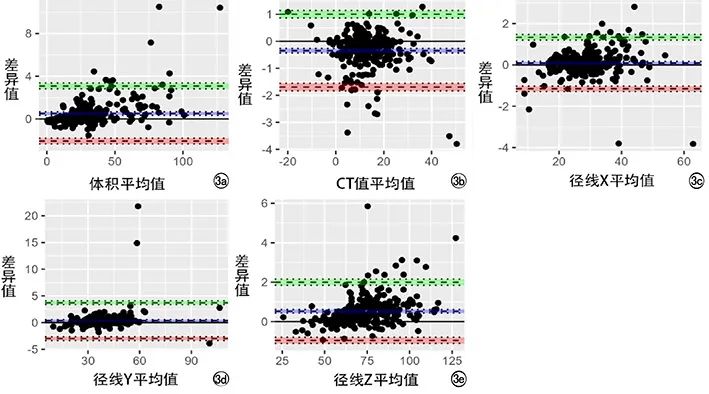
图3 胆囊区域测量值的Bl
and-Altman分析。a)体积;b)CT值;c、d、e)三维径线的95% LoA的可信区间分别为(-2.07,3.36)、(-1.55,1.15)、(-1.28,1.47)、(-3.34,4.07)和(-1.11,2.15),分别有2.6%、3.7%、3.7%、1.1%和3.7%的点落在95%LoA以外。
讨论
胆囊是一个薄壁的肌性和膜性囊腔,一般情况下容积
20-30ml,长度7-10cm,宽度3cm。位于肝右叶下面的陷窝内。随着胆囊疾病的发病率和患病率上升,胆囊的影像评估成为腹痛患者检查的重要组成部分。胆囊成像的影像学方法包括超声(ultrasonography,US)、计算机断层扫描(computed- tomography,CT)、磁共振(magnetic resonance imaging,MRI)成像和核闪烁成像。既往认为超声是胆囊疾病的首选检查方式, 现在CT已经成为其主要检查手段。本研究基于3D U-Net分割模型,实现了在CT图像上分割胆囊轮廓,并借助最小体积包围盒、保留像素数等算法自动输出胆囊的三维径线、体积和 CT 值等,初步研究CT 图像上胆囊分割及自动测量的可行性。
近年来,深度学习在医学图像分割上广泛应用,但是基于腹部CT胆囊分割的研究相对较少。Lian等基于区域生长实现在超声图像的胆囊及结石的分割。华中科技大学团队提出胆囊半自动交互式分割,该方法需使用者手动选定部分区域。尹梓名等提出基于注意力机制的 Attention U-Net模型,优化模型胆囊分割表现。本研究采用的3D U-Net模型,相较于传统图像分割仍需要人工设计提取相应特征,本研究基于神经卷积网络可自动提取图像特征,分割效能明显提高。U-Net 是Ronneberger等于2015年提出的,Cicek等于2016年进一步提出了3D U-Net网络,该网络在很多器官的分割任务中表现出色。本研究结果证明尽管胆囊形态体积及胆囊内密度的高度可变,采用3D-U Net网络可以更好的观察胆囊整体,不局限于2D平面,对阅片者提供胆囊相应径线及CT
值等相关定量信息。
应注意的是虽然整体分割效能很好,但仍有少量数据胆囊分割欠满意,在141例外部验证数据中29例分割欠满意,具体原因:15例术后将邻近肠管或积液误认;7例胆因囊密度增高未识别出,1例脂肪肝患者未识别出;5例标签识别范围包含邻近肝囊肿、门静脉等;1例胆囊炎囊壁水肿明显,未识别完整。考虑到胆囊周围毗邻脏器较多,背景杂乱;在不影响疾病诊断的前提下,胆囊部分边界分割欠清,目前这样的分割结果是对于显示胆囊可以接受的,但对于胆囊测量是不合格的。未来应增加多种疾病状态下的胆囊图像迭代训练模型以进一步提高分割效能。
当前,胆囊分割模型可在实际工作中用于胆囊的定量测量。在腹部CT疾病的影像诊断过程中,影像医师要先定位出胆囊;继而通过测量分析胆囊的大小、形态、密度等影像信息,判断胆囊整体正常与否,若有异常进一步评判病变范围并尽可能定性诊断,为下一步临床治疗决策提供可靠依据。胆囊的分割是胆囊疾病诊断的第一步,深度学习分割模型遵循常规诊断思路,可帮助快速正确分割胆囊区域,辅助判别有无胆囊存在,可避免胆囊术后仍正常描述胆囊的情况出现。而基于人工的影像学测量耗费时间长、可重复性低,人为误差大,基于深度学习的自动测量缩短测量时间,提高测量的可重复性。
未来,应在胆囊自动分割的基础上增加胆囊疾病检出和诊断的模型。本研究应用深度学习的方法对胆囊分割的结果较为理想,为临床提供了大量定量信息。今后可在此基础上进一步测量胆囊结石、胆囊炎粘连程度、胆囊壁厚度等,更大程度发挥其临床应用价值。胆囊的大小和密度可以反应胆囊浓缩、排出胆汁的功能。 餐后胆囊、慢性胆囊炎可以表现为胆囊体积减小;而急性胆囊炎胆囊体积增大。胆汁淤积、阳性胆囊结石胆囊腔内密度增高。本模型为后续疾病的诊断随访提供潜在的临床价值。
本研究仅为初步探索,仍存在许多不足之处。第一,本模型是一个单中心回顾性研究,在证明模型泛化性能上有一定局限性,后续模型推广使用过程中应进行多中心研究。第二,数据包含胆囊疾病谱不足,部分少见胆囊疾病,如胆囊结肠瘘、黄色肉芽肿性胆囊炎等未纳入数据组。
综上所述
,初步研究结果显示基于深度学习模型可在CT图像上自动分割并测量胆囊,与专家测量水平基本一致。未来可以这个分割模型为基础进一步研发胆囊疾病的诊断模型以实现临床价值。
作者单位:1.北京大学第一医院医学影像科,北京 100034;
2.首都医科大学基础医学院,北京 100069;
3.北京赛迈特锐医学科技有限公司,北京 100011