优化候选药物性质时,后期功能化Late-stage functionalizatio是一种经济方法。然而,药物分子的化学复杂性,往往使后期多样化极具挑战。
近日,世界著名医药企业之一 瑞士 罗氏有限公司(F.Hoffmann-La Roche Ltd.)David F. Nippa,Rainer E. Martin等,苏黎世联邦理工学院 (ETH Zurich) Kenneth Atz, Uwe Grether, Gisbert Schneider等,在Nature Chemistry上发文,报道开发了基于几何深度学习和高通量反应筛选的后期功能化平台。考虑到硼化borylation是后期功能化的关键步骤,计算模型预测了不同反应条件时的反应产率,平均绝对误差为4–5%,而对已知和未知底物新反应的反应性进行了分类,平衡准确度分别为92%和67%。准确捕获了主要产物的区域选择性,分类器F分数为67%。当应用于23种不同商业药物分子时,该平台成功地确定了许多结构多样化机会。量化了空间和电子信息对模型性能的影响,并介绍了一种全面、简单、用户友好的反应格式,并证明是无缝集成深度学习和高通量实验,以实现后期功能化的关键因素。 Enabling late-stage drug diversification by high-throughput experimentation with geometric deep learning. 基于几何深度学习,高通量实验实现了后期药物多样化。
Enabling late-stage drug diversification by high-throughput experimentation with geometric deep learning. 基于几何深度学习,高通量实验实现了后期药物多样化。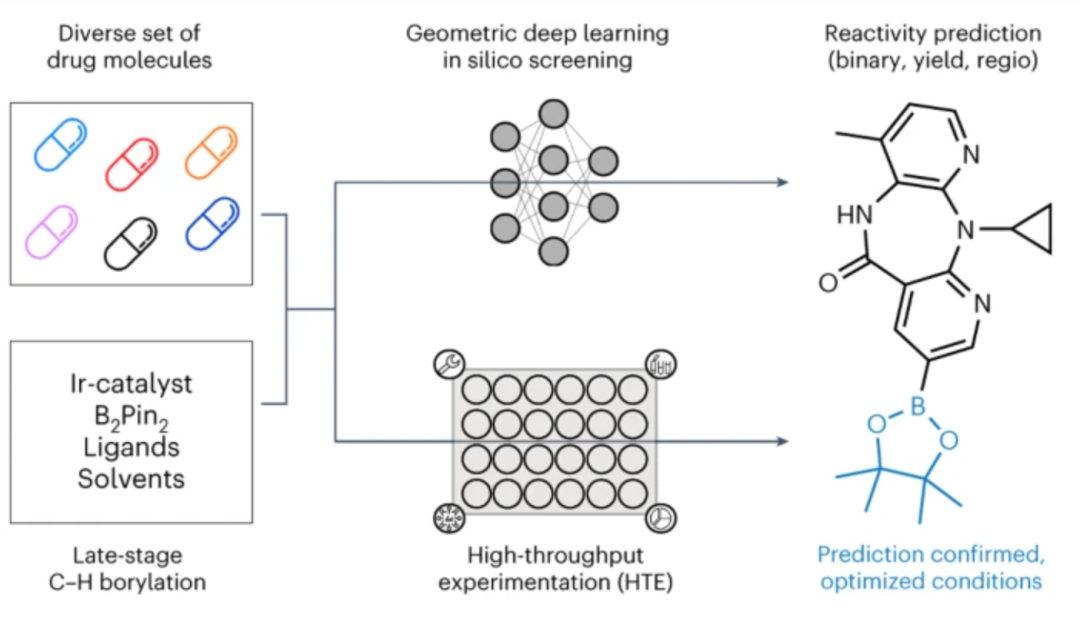
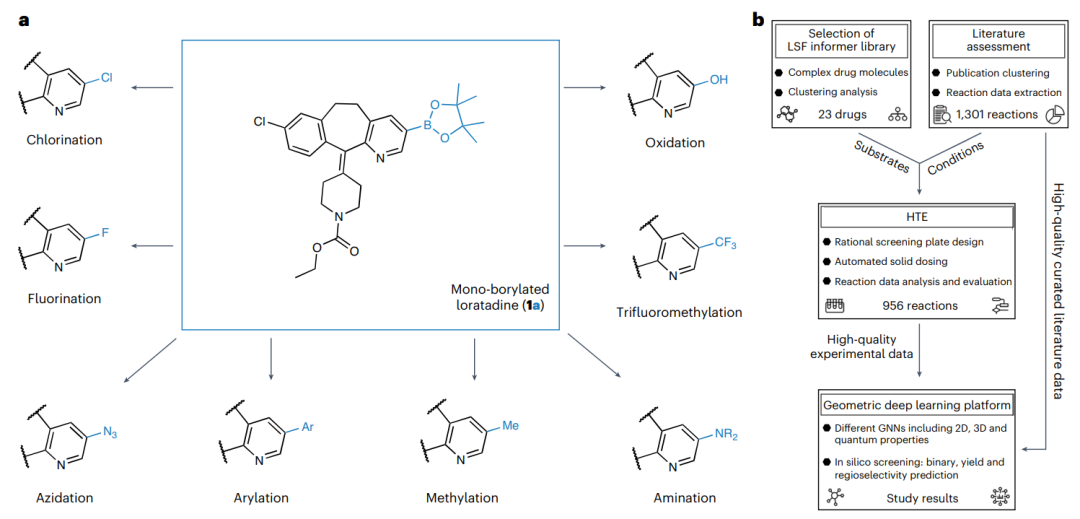
图1: 硼化多样化机会和研究概述。
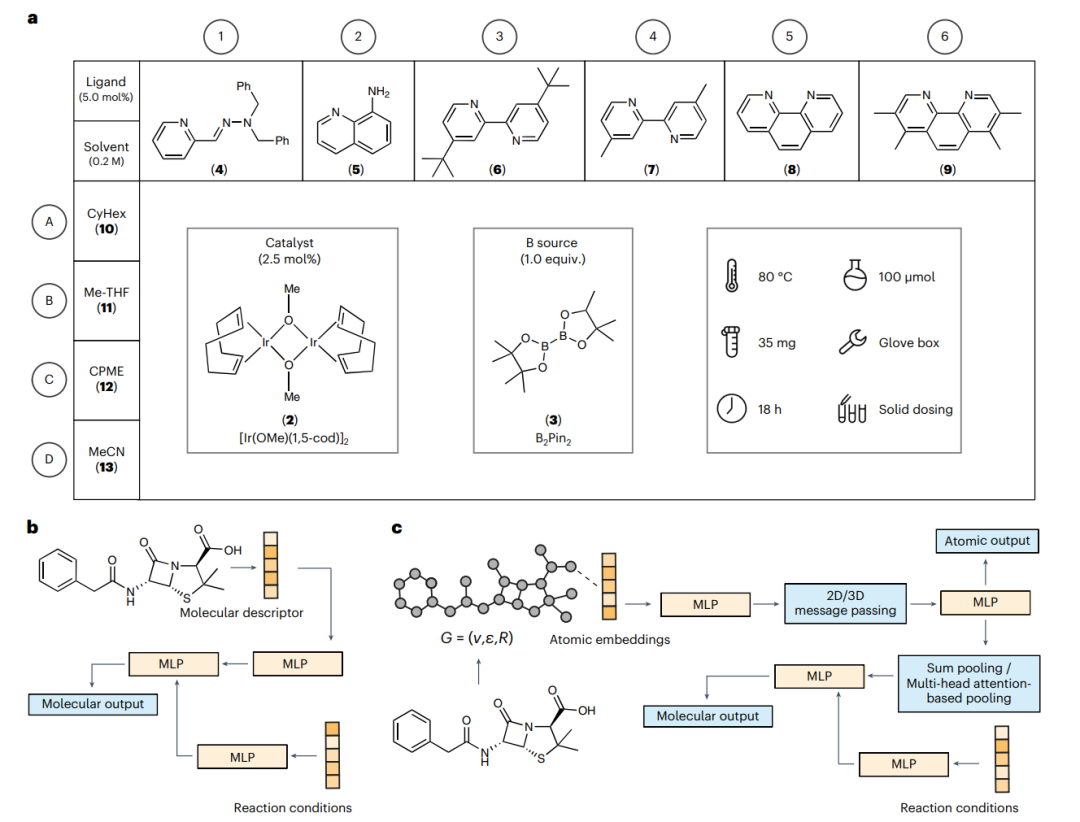
图2: 筛选板Screening plate和图神经网络Graph neural networks,GNN架构。
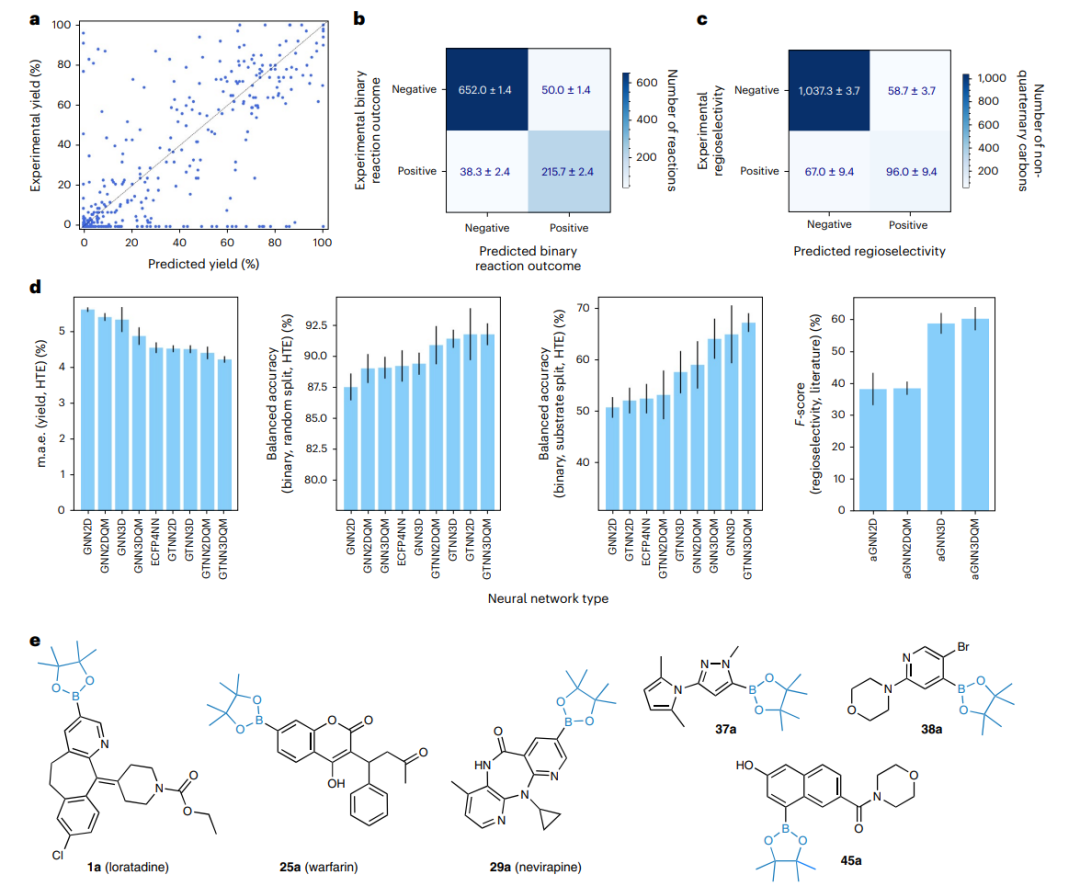
图3: 二元反应产物、反应产率和区域选择的预测结果。
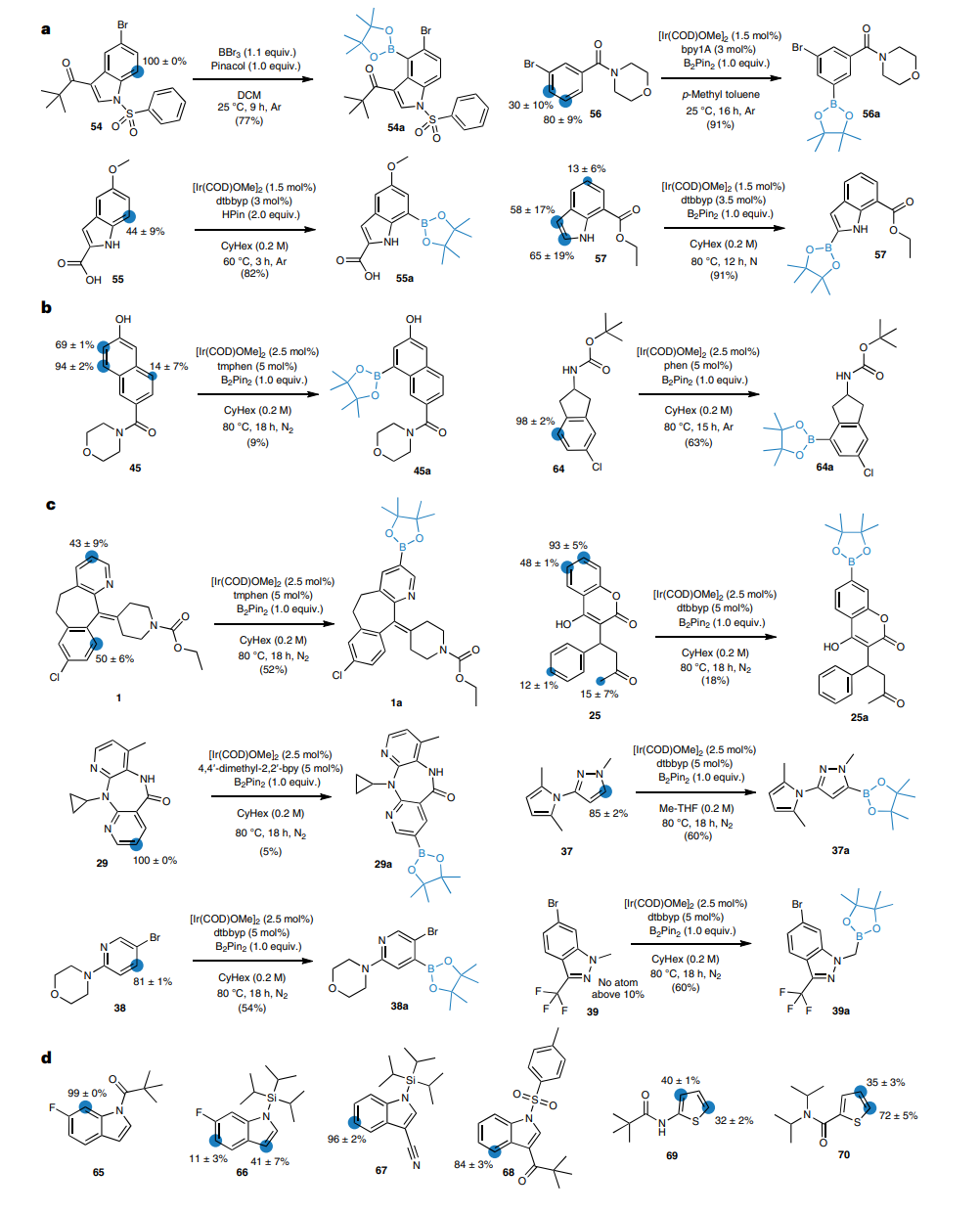
图4: 硼化区域选择性预测的实例。
Nippa, D.F., Atz, K., Hohler, R. et al. Enabling late-stage drug diversification by high-throughput experimentation with geometric deep learning. Nat. Chem. (2023). https://doi.org/10.1038/s41557-023-01360-5https://www.nature.com/articles/s41557-023-01360-5https://www.nature.com/articles/s41557-023-01360-5.pdf声明:仅代表译者个人观点,小编水平有限,如有不当之处,请在下方留言指正!