 2021年12月10日,罗氏宣布,靶向TIGIT的新型癌症免疫疗法tiragolumab,联合PD-L1抑制剂阿替利珠单抗(atezolizumab),在一线治疗PD-L1阳性转移性非小细胞肺癌(NSCLC)患者的2期临床试验(CITYSCAPE)中获得积极结果。结果将在2021年12月8-11日召开的ESMO Immuno-Oncology 大会上口头报告。在中位随访时间为2.5年时,与阿替利珠单抗单药治疗相比,tiragolumab+阿替利珠单抗组合的无进展生存期(PFS)获得显著改善。
2021年12月10日,罗氏宣布,靶向TIGIT的新型癌症免疫疗法tiragolumab,联合PD-L1抑制剂阿替利珠单抗(atezolizumab),在一线治疗PD-L1阳性转移性非小细胞肺癌(NSCLC)患者的2期临床试验(CITYSCAPE)中获得积极结果。结果将在2021年12月8-11日召开的ESMO Immuno-Oncology 大会上口头报告。在中位随访时间为2.5年时,与阿替利珠单抗单药治疗相比,tiragolumab+阿替利珠单抗组合的无进展生存期(PFS)获得显著改善。
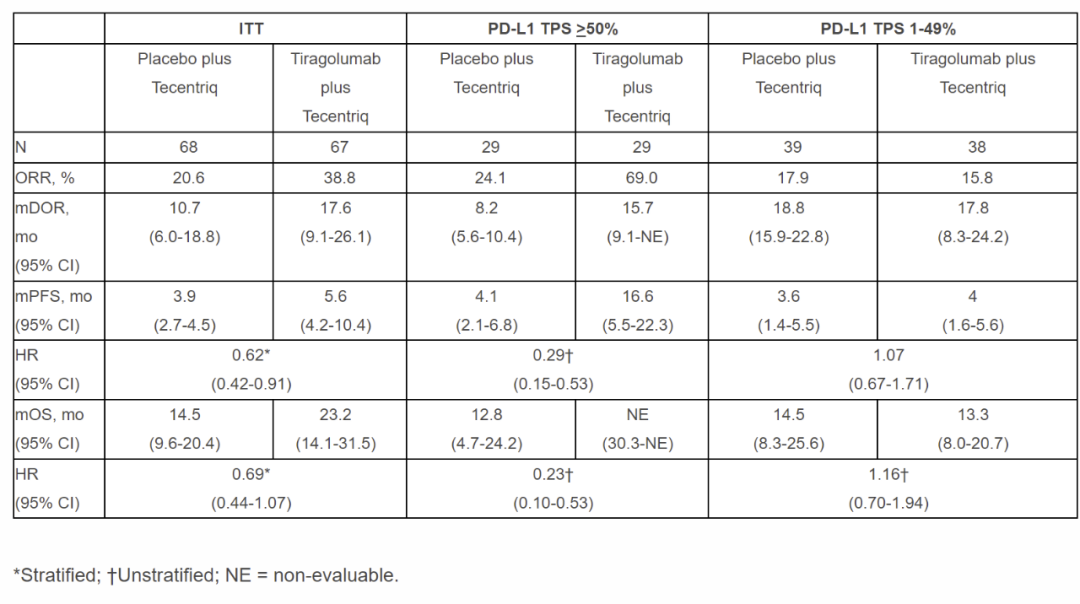
TIGIT(T cell immunoreceptor with Ig and ITIM domains)全称为T细胞免疫球蛋白和ITIM结构域蛋白,是主要在T细胞和自然杀伤(NK)细胞表面表达的免疫检查点蛋白。用tiragolumab阻断TIGIT信号通路,有可能增强机体对癌细胞的免疫反应,提高抗肿瘤活性。CITYSCAPE是一项全球II期、随机、盲法研究,旨在评估135例PD-L1一线阳性局部晚期、不可切除或转移性非小细胞肺癌患者,使用tiragolumab+阿替利珠单抗或单独使用阿替利珠单抗的有效性和安全性。患者按1:1随机分为两组,一组接受iragolumab+阿替利珠单抗治疗,另一组接受安慰剂+阿替利珠单抗治疗,直至病情进展或无临床疗效。共同主要终点是总有效率(ORR)和无进展生存率(PFS)。次要终点包括安全性、总生存率(OS)和患者报告的结果(PRO)。PRO结果使用EORTC QLQ-C30进行评估,该问卷用于评估癌症患者的生活质量,在基线和整个研究治疗期间进行。最新结果显示,在中位随访时间为 2.5年时:在意向治疗(ITT)人群(n=67)中,与阿替利珠单抗单药治疗(中位PFS=3.9个月)相比,tiragolumab/阿替利珠单抗组合使患者疾病进展或死亡的风险降低了38%,中位PFS为5.6个月(HR=0.62,95% CI:0.42–0.91),并提高了总缓解率(ORR)(38.8% VS. 20.6%)。在PD-L1高表达(TPS≥50%)患者(n=29)中进行的探索性分析显示,与阿替利珠单抗单药治疗(中位PFS=4.1个月)相比,患者疾病进展或死亡风险的风险降低了71%,中位PFS为16.6个月(HR=0.29,95% CI:0.15–0.53),ORR显著改善(69% VS. 24.1%)。 在总生存期(OS)的试验次要终点上,tiragolumab+阿替利珠单抗组合也为ITT人群带来获益,中位OS为23.2个月(对照组为14.5个月)(HR=0.69,95% CI:0.44–1.07)。
安全性方面,联合用药总体上耐受性良好,与单独使用阿替利珠单抗相比,tiragolumab+阿替利珠单抗的3-4级治疗相关不良事件(AE)发生率相似(联合组22.4%vs 单药组25%)。联合用药最常见的全因不良事件(大于5%)是输液相关反应、强直、皮肤干燥、疲劳和皮疹。经过更长时间的随访,联合用药未观察到新的安全信号。与治疗开始时相比,患者通常报告有轻微至中度症状,并总体维持其生活质量。来自该探索性分析的PRO数据表明,在联合治疗组,肺部症状,如呼吸困难和疼痛,似乎没有恶化。Phase II 临床试验中,67例联合治疗患者的有效性数据令人鼓舞,PFS HR 0.62值得期待,毫无疑问,tiragolumab与阿替利珠单抗联合治疗一线NSCLC,还需要更大样本量的phase III临床试验进一步夯实结果,因为phase II数据亮眼,但到了扩大样本量的phase III结果“翻车”的案例并不罕见。
参考文献:
Roche - New data from the phase II CITYSCAPE trial show encouraging results with Roche’s novel anti-TIGIT tiragolumab plus Tecentriq
识别微信二维码,添加抗体圈小编,符合条件者即可加入抗体圈微信群!

本公众号所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系(cbplib@163.com),我们将立即进行删除处理。所有文章仅代表作者观点,不代表本站立场。
